为深化“放管服”改革,优化营商环境,进一步提升医疗器械注册工作的效率与透明度,国家药品监督管理局(NMPA)持续推进医疗器械注册电子申报信息化系统(以下简称“eRPS系统”)的建设与应用。为规范系统使用,保障相关业务顺利办理,现将有关事宜通告如下:
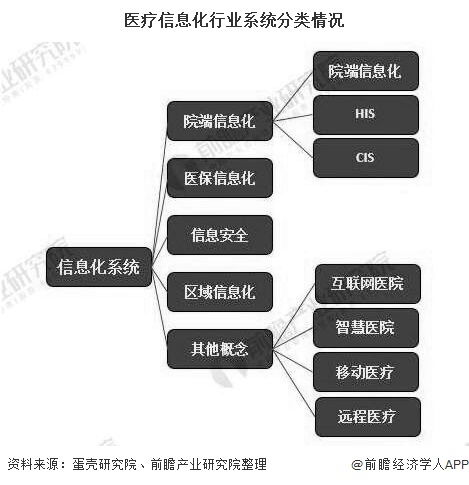
一、 系统功能与适用范围
医疗器械注册电子申报信息化系统是一个集在线申报、资料提交、受理审查、进度查询、电子证照发放于一体的综合性服务平台。自本通告发布之日起,该系统正式全面应用于境内第三类医疗器械产品注册、变更注册、延续注册,以及进口第二类、第三类医疗器械产品的相应注册事项。鼓励注册申请人优先采用电子途径提交申请。
二、 用户注册与身份认证
注册申请人需通过国家药监局网上办事大厅进行法人用户实名注册与认证。完成认证后,即可登录eRPS系统进行业务操作。申请人应妥善保管账号及密码,确保申报行为真实、有效,并对所提交电子资料的法律效力负责。
三、 申报资料准备与提交要求
- 格式标准:申报资料应严格按照《医疗器械注册申报资料要求及说明》进行准备,并以系统规定的结构化电子文档格式(如PDF、WORD等)上传。文件应清晰、完整,符合电子档案管理规范。
- 签章要求:所有需要盖章或签字的文件,均应使用符合《中华人民共和国电子签名法》要求的可靠电子签名或电子签章。
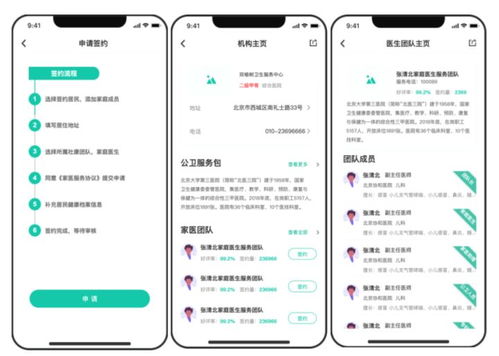
- 提交流程:申请人登录系统后,按照指引在线填写申请表、上传申报资料,确认无误后正式提交。系统将自动生成受理号及提交回执。
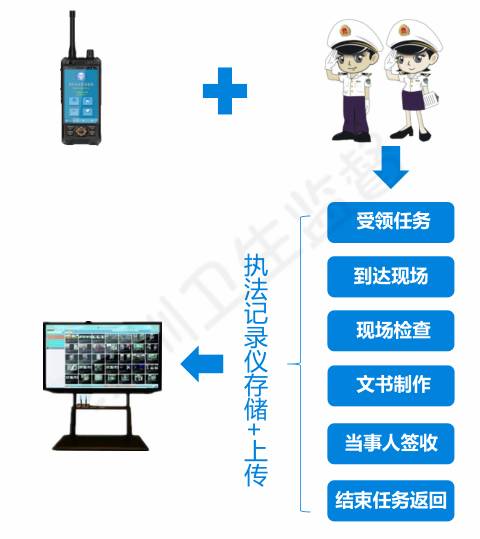
四、 受理审查与进度查询
药品监督管理部门在收到电子申报后,将依据法规时限进行受理审查。申请人可随时通过eRPS系统实时查询申请状态、补正通知、审评进度及最终审评结论。系统将自动推送关键节点信息,实现办理过程全流程可追溯。
五、 电子证照发放
对于予以批准的注册事项,药品监督管理部门将通过eRPS系统直接发放医疗器械注册证、变更文件等电子证照。电子证照与纸质证照具有同等法律效力。申请人可登录系统下载、打印和使用。确需纸质证照的,可另行申请。
六、 过渡期安排与咨询服务
为保障平稳过渡,系统上线初期将设置为期三个月的并行期。在并行期内,申请人仍可选择传统纸质方式提交申请,但鼓励优先使用电子申报。并行期结束后,通告范围内的事项原则上将全面采用电子申报。
系统使用过程中如遇技术问题,可联系技术支持热线(示例:010-12345678)或通过系统在线客服咨询。有关法规与业务问题,请咨询相应业务主管部门。
特此通告。
国家药品监督管理局
XXXX年XX月XX日